نظارت بر سیستم های هوای فشرده شرکت های داروسازی مطابق با استاندارد GMP
گاز های فشرده در استفاده مستقیم در تولید مواد دارویی و در کنترل فرآیند های مربوطه،
به سطح بالایی از دقت و یکپارچگی با روش های خوب تولید،
که با عنوان استاندارد GMP یا Good Manufacturing Practices شناخته شده است، در تکنولوژی اتاق تمیز نیاز دارد.
ممکن است تأمین نیتروژن فشرده در مخازن تحت فشار به صورت گاز و یا مایع تهیه شود
و دارای گواهی آنالیز CoA نیز باشد تا بر کیفیت این گاز صحه گذاری کند،
اما کیفیت سنجی هوای فشرده ای که در یک سایت مشخص تولید می شود،
به راحتی امکان پذیر نیست چرا که منبع اصلی تولید هوای فشرده، هوای محیط می باشد
که در مکان های مختلف این هوای محیط کاملا متفاوت بوده و به شدت از عوامل محیطی تاثیر می پذیرد
و تاثیر مستقیم بر کیفیت هوای فشرده تولید شده دارد.
فشرده سازی با استفاده از هوای محیط به عنوان یک منبع انجام می شود که می تواند در مکان های مختلف بسیار متفاوت باشد
همچنین می تواند به شدت تحت تأثیر اثرات محیطی قرار گیرد که بر کیفیت تاثیر مستقیم دارد
تنها استفاده از یک فیلتراسیون مناسب بعد از مرحله تولید هوای فشرده می تواند کیفیت هوای فشرده را در پروسه توزیع و نقاط مصرف تضمین کند.
برای تحقق این مهم، اطلاعات لازم در خصوص کاربرد آن هوای فشرده، یک سیستم تصفیه و توزیع هوای فشرده معتبر،
و مهم تر از همه یک سیستم مانیتورینگ مناسب برای اندازه گیری پارامترهای مهم که مطابق با روش های اندازه گیری مورد تایید در استانداردهای مربوطه باشد، مورد نیاز می باشد.
هوای فشرده در داروسازی ها طبق استاندارد GMP
هوای فشرده، “ماده ای گران قیمت” است
نه تنها وقتی که به هزینه های استفاده از انرژی برای کار کردن یک شبکه هوای فشرده به شیوه ای مطمئن نگاه می کنید.
بلکه هوای فشرده از این حیث هم بسیار ارزشمند است زیرا اغلب بیش از حد انتظار به صورت مستقیم با تولید محصول نهایی درگیر می شود.
هوای فشرده به طور خاص در فرآیند هایی مانند:
خارج کردن هوا از بسته بندی اولیه (blowing out primary packaging)، حمل محصولات از ظرف به سوزن پر کننده در شرایط آسپتیک،
خشک کردن مخازن و ظروف نگهداری دارویی و یا تخلیه هوا پس از ایجاد خلاء زیاد در لیوفیلیزرها یا تخمیر کننده ها کاربرد دارد.
از آنجا که هوای فشرده تاثیر بسیار مهم و کلیدی بر روی کیفیت محصول نهایی تولید شده دارد،
بنابراین نیازمند توجه بسیار بالایی در سیستم GMP1,2می باشد.


در گزارش های متعدد در بازرسی های رسمی در خصوص کیفیت گازهای فشرده در داروسازی ها، معمولا انتقاد می شود
که گزارشات با مشخصات واضح ثبت نشده است
و صلاحیت پایدار و مدیریت GMP در مورد عملکرد گازهای فشرده احراز و اعمال نشده است.
به بیانی دیگر، یا گزارشات در این خصوص با اطلاعات لازم ایجاد نشده یا به طور ناکافی انجام شده اند.
دلیل این امر مطمئناً این است که برای هوا، برخلاف سیالات مایع مانند آب تصفیه شده یا آبی که برای تزریقات استفاده می شود،
هیچگونه مشخصات روشنی توسط فارماکوپه اروپا (Ph.Eur) وجود ندارد.
مشخصات کیفیت هوای دارویی که در فارماکوپه اروپا یافت می شود، برای استفاده در هوای فشرده نامناسب است؛
زیرا این استاندارد صرفا کیفیت هوای تنفسی ارائه شده به بیمار را با معیار های مورد قبول توصیف می کند.
استاندارد ISO 8573-3 از سازمان بین المللی استاندارد نیز در این زمینه کاربرد محدودی دارد؛
زیرا در اینجا طبقه بندی مقادیر مجاز برای غلظت ذرات، نقطه شبنم فشار و میزان روغن هوای فشرده تعریف شده است
اما ذکر نشده است که در کدام بخش داروسازی و طبق کدام کلاس یا مشخصات باید استفاده شود.
ISO 8573 همچنین در مورد مشخصات احتمالی میکروب های موجود در هوا مشابه ضمیمه 1 دستورالعمل GMP اتحادیه اروپا چیزی نمی گوید.
این واقعیت به عنوان یک روند در ماه های اخیر در جریان بازرسی های رسمی مورد توجه قرار گرفته است.
بنابراین گاز های فشرده نیتروژن و هوای فشرده به نقطه تمرکز این نظارت ها تبدیل شده اند.
اطلاعات بیشتر: نظر رسمی در مورد ارزیابی الزامات استاندارد GMP برای سیستم های هوای فشرده در “Aide Memorie تحت عنوان نظارت بر تولیدکنندگان استریلیزه” در دفتر مرکزی ایالات فدرال برای حفاظت از سلامت در آلمان (4) منتشر شد.
در این نظر آمده است:
“هنگام تعیین هوای فشرده که در تماس با محصول یا سطوحی که با محصول در تماس هستند ،
علاوه بر نوع محصولات تولید شده، ارزیابی ریسک باید طراحی سیستم و کیفیت خروجی هوای فشرده را نیز در نظر بگیرد.”


در رابطه با ارزیابی هیدروکربن ها، باید توجه داشت که آلودگی به روغن در هوای فشرده،
مخلوطی از آئروسل ها یا بخارات روغن و سایر هیدروکربن ها است.
بنابراین تعریف “روغن”به عنوان مخلوطی از هیدروکربن ها با 6 اتم کربن یا بیشتر مطابق با استاندارد ISO 8573-1 نسخه 2010 مناسب است.
بنابراین متد های اندازه گیری میزان روغن و نیز اجزای روغن ثبت شده باید روشن شوند.
نظارت بر هیدروکربن برای کمپرسور های هوای بدون روغن(oil-free air compressors) نیز ضروری است؛
زیرا آلاینده های مربوطه نیز از طریق هوای ورودی به کمپرسور وارد هوای فشرده می شوند.
پارامتر های خلوص زیر که در ISO 8573 شرح داده شده است، باید مورد توجه قرار گیرد:
- مقادیر مجاز برای تعداد یا ذرات باکتریایی پیش بینی و تعیین می شود.
- نظارت آنلاین بر آب و هیدروکربن ها ممکن است ضروری باشد.
به ویژه برای سیستم هایی که به دلیل استفاده از خشک کن های تبریدی(Refrigeration Dryers)
یا کمپرسور های هوا با سیستم خنک کننده روغن(air compressors with oil cooling) خطر عدم رعایت مشخصات مورد نیاز بیشتر است.
با این توضیح ، هیچ محدودیت مقداری مطابق با تعریف استاندارد ISO 8573 در موارد مذکور وجود ندارد.
اما جهت و حدود آن مشخص است. به منظور تعریف و تعیین مشخصات مورد نیاز توصیه می شود
که طبقه بندی را بر اساس انجمن تولیدکنندگان ماشین آلات و کارخانجات آلمان (VDMA) بسته به کاربرد (حساسیت محصول) انجام دهید.
به عنوان مثال هنگام استفاده در منطقه استریل،
“تماس مستقیم هوای فشرده با مواد بسته بندی استریل (هوای فرآیند)” در بخش 5 استاندارد VDMA 15390 با معیار های زیر تعریف شده است:
- حداکثر اندازه ذرات و چگالی آلاینده های جامد:
کلاس 1، برابر است با اندازه ذرات 0.1 میکرومتر و چگالی 0.1 میلی گرم بر متر مکعب. - نقطه شبنم فشار در دمای محیطی بالاتر از 10 درجه سانتیگراد:
کلاس 4، برابر با 3 درجه سانتیگراد Td(+ 3°C Td) است. - نقطه شبنم فشار در دمای محیطی کمتر از 10 درجه سانتیگراد:
کلاس ۲ یا ۳ که به ترتیب منفی 40 درجه سانتیگراد Td و منفی 20 درجه سانتیگراد Td (-40°C Td /-20°C Td ) است. - حداکثر میزان روغن:
کلاس 1، برابر با 0.01 میلی گرم در مترپ مکعب است. - شرایط استریلیزه بودن:
بله
خطرات آلودگی در هوای فشرده
به عنوان استدلال اصلی برای ایمنی در استفاده از هوای فشرده در محیط GMP،
بارها در شرایط بازرسی توسط بازرسین نشان داده می شود
که استفاده از کمپرسور های هوای فشرده بدون روغن برای اطمینان از هوای فشرده واجد شرایط و بدون آلودگی کافی است.
متاسفانه این یک باور اشتباه است؛
زیرا خطر آلودگی اغلب به طور قابل توجهی بیشتر از حد انتظار یا شناخته شده است.
به بیانی ساده تر می توان آن را به دو حوزه تقسیم کرد:
- آلودگی فعال در سیستم تصفیه هوای فشرده
- آلودگی غیرفعال هوای فشرده با مصرف کننده هایی که به شبکه هوای فشرده متصل شده اند.
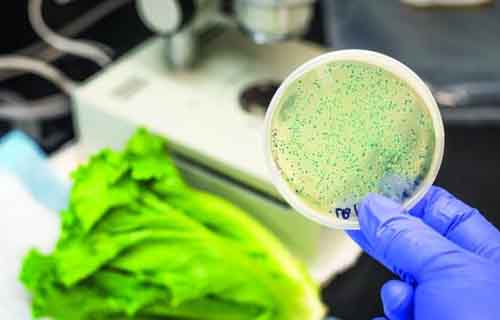

در مورد آلودگی های فعال، علت اصلی آلودگی، استفاده از کمپرسور های هوا با سیستم خنک کاری روغن یا اویل اینجکت است.
اما علاوه بر آن، آلاینده های دیگر را باید در هوای محیط جستجو کرد
که به عنوان منبع اصلی تولید هوای فشرده به داخل کمپرسور مکش می شود.
بسته به موقعیت دهانه ورودی هوای کمپرسور،
میزان قابل توجهی ذرات و آلاینده های روغنی به شکل آئروسل(بخارات) می توانند از هوای محیط وارد کمپرسور شده و فشرده شوند.
آلودگی های عمدتا جزئی که به شکل ذرات و روغن توسط قسمت های متحرک کمپرسور هوا ایجاد می شوند،
به ویژه پس از یک دوره طولانی کار کمپرسور، نیز بایستی مورد توجه قرار گیرد.
علاوه بر این رطوبت زیادی از طریق هوای محیط وارد کمپرسور می شود
و باعث ورود بالقوه میکروب های هوا به سیستم در حال کار و در نتیجه به شبکه خط لوله هوا می شود.
در مورد آلودگی غیر فعال، خطری که کیفیت هوای فشرده را تهدید می کند این است که:
به دلیل عوامل نامساعد یا ابعاد نامناسب لوله،
مصرف کنندگان بزرگ در سیستم هوای فشرده باعث برگشت فشار بیش از حد در خطوط هوای فشرده شده که منجر به ایجاد خلاء در سیستم می شود.
در مورد تهویه استریل با استفاده از هوای فشرده بیایید یک مثال بزنیم.
به عنوان مثال مخازنی که پس از تمام شدن فاز بخار،
پس از استریل سازی با بخار یا هنگامی که خلاء زیاد لیوفیلیزرها هنگام باز شدن شیر به خطوط هوای فشرده افت می کند،
وارد فاز خلاء می شوند، باعث معکوس شدن فشار در سیستم هوای فشرده می شوند.
خطر اصلی در اینجا این است که ممکن است در بدترین حالت چنین فشار منفی موقت و بزرگی در شبکه هوای فشرده ایجاد شود
که آلودگی برگشتی به سیستم از طریق خطوط هوای فشرده توسط سایر مناطق عملیاتی رخ دهد.
هنگام طراحی شبکه های هوای فشرده، قبل از اتصال مصرف کنندگان جدید، این امر باید کاملاً بر اساس ریسک احتمالی بررسی و برنامه ریزی شود.
یا در فرآیند کنترل تغییرات داخلی در نظر گرفته شود.
برای جلوگیری از چنین اثراتی، می توان از مدارهایی به نام بلاک اند بلید (Block & Bleed Circuits)
و یا نصب شیرهای کنترلی در خطوط هوای فشرده استفاده کرد.
در هر صورت، این مورد نیز باید به عنوان بخشی از صلاحیت نصب (Installation Qualification(IQ
یا صلاحیت عملکرد OQ) Operational Qualification) مطابق با استاندارد GMP بررسی شود.
حال برای هر دو آلودگی فعال و غیر فعال بررسی می کنیم:
در اغلب شبکه های هوای فشرده دارای انشعابات بسیار گسترده در یک کارخانه داروسازی، این اصل اعمال می شود:
“آنچه در شبکه وجود دارد، در آنجا باقی می ماند!”
در بیشتر موارد، یا پاکسازی آلودگی امکان پذیر نیست یا اغلب در برنامه ریزی هوای فشرده در نظر گرفته نمی شود.
برای اینکه سطح آلودگی در خطوط هوای فشرده به طور کلی قابل مشاهده و یا کنترل باشد،
توصیه می شود که یک لوله به نام لوله بازرسی (Inspection Pipe) نصب شود.
یعنی یک لوله با طول تقریباً 50 – 100 سانتیمتری که می توان با استفاده از اتصالات سه گیره tri-clamp connections به عنوان بخشی از تعمیر و نگهداری های برنامه ریزی شده، برداشته و بازرسی شود.
در موارد شدید، میزان آلودگی می تواند منجر به نوسازی جزئی یا کامل یا جایگزینی کامل شبکه هوای فشرده شود.


احراز صلاحیت(Qualification) سیستم های هوای فشرده و توزیع هوای فشرده بر اساس استاندارد GMP
یکی از سوالات متداول هنگام بررسی سیستم های هوای فشرده،
نیاز به احراز صلاحیت کامل تمام اجزای تولید و توزیع هوای فشرده است.
اولین مشکل در اینجا این است که برخلاف یک کارخانه فرآیندی (به عنوان مثال خط پرکن برای پروسه های اسپتیک) برنامه ریزی مطابق GMP با در نظر گرفتن طراحی بهداشتی hygienic design برای کمپرسور هوا تقریباً غیرممکن است.
حتی اگر کمپرسور های هوا گاهی اوقات با اشاره به عملکرد بدون روغن توسط سازنده سازگار با استاندارد GMP تلقی شوند،
این به طور کلی فقط به عدم وجود سیستم خنک کاری توسط روغن و کاهش قطعات روان کننده یا آزاد کننده ذرات اشاره می کند.
بنابراین یک عمل به رسمیت شناخته شده GMP این است که کمپرسور هوا،
از جمله نصب آن، از نظر فنی باید منطبق با قوانین روشهای مهندسی خوب (Good Engineering Practice (GEP باشند
که همه اسناد مربوطه فنی ارائه شده اند و راه اندازی موفق نیز مستند شده است.
در این زمینه، مدارک IQ / OQ کلاسیک نسبتاً نامناسب به نظر می رسد.
این مورد باید در طرح جامع اعتبار سنجی (VMP) شرکت GMP تحت عنوان GMP در مقابل GEP فهرست شده یا تعریف شود.
این رویکرد توسط ISPE در سال 2014 اتخاذ شد
و دستور العمل های خوب گازهای فرآیندی در انجمن بین المللی مهندسی داروسازی (ISPE) نیز به شرح زیر توضیح داده شد:
تولید گاز به طور معمول از شیوه های مهندسی خوب (GEPs) پیروی می کند.
گاز یک محصول دارویی نیست و نیازی به تولید آن مطابق با شیوه های خوب تولید Good Manufacturing Practices نیست.


از نظر GMP آماده سازی کیفی هوای فشرده حائز اهمیت میباشد تا تاثیر منفی بر روی مشخصات مورد نظر نداشته
و برای استفاده در فرایند مربوطه مناسب باشد.
مناسب بودن تمام اجزای مورد نیاز برای آماده سازی و توزیع در مراحل IQ ,DQ و OQ و نیز یک صلاحیت عملکرد کافی
(Performance Qualification) PQ، یک بخش اجباری از احراز صلاحیت / اعتبارسنجی هوای فشرده است
و به عنوان یکی از پیامد های GMP منوط به انحراف یا تغییر سیستم مدیریتی است.
در قیاس با روش GMP/GEP، توزیع و پردازش هوای فشرده، که منحصراً برای مصارف فنی در خارج از اتاق تمیز استفاده می شود،
که به معنی عدم تماس مستقیم یا غیر مستقیم با محصول است،
دوباره می تواند به عنوان یک سیستم GEP در نظر گرفته شود.
بنابراین تابع قوانین احراز صلاحیت رسمی نیست.
در حین احراز صلاحیت، باید توجه ویژه ای به تجهیزات فرایندی متصل / مصرف کنندگان هوا شود.
در اینجا نیز باید اطمینان حاصل شود که فشار اضافی یا شرایط خلاء درون فرآیند هیچ تاثیری منفی بر روی سیستم هوای فشرده
و لوله های داخلی سیستم به دلیل خطر برگشت آلاینده ها به سیستم لوله کشی ندارند.
نقطه مرزی سیستم برای احراز صلاحیت در سیستم هوای فشرده باید نقطه انتقال هوا به سیستم فرآیند باشد.
به عنوان مثال سنسور نظارت بر فشار یک سیستم فرآیندی نیز برای احراز صلاحیت بررسی می شود
و در صورت لزوم باید تحت کالیبراسیون منظم قرار گیرد.
بازرسی کیفی یا نمونه گیری از هوای فشرده
با طبقه بندی هوای فشرده به عنوان یک سیال مهم در پروسه های دارویی،
بررسی منظم کیفیت هوای فشرده مطابق با مشخصات مورد نظر، جزء ضروری سیستم اعتبار سنجی است.
همانند سیستم های آب داروسازی ها، باید نمونه نقشه ای به عنوان بخشی از PQ(احراز صلاحیت عملکرد) برای عملیات جاری پس از راه اندازی تهیه شود.
تعداد نقاط نظارت و دفعات نمونه گیری باید براساس تجزیه و تحلیل ریسک، تعیین و برنامه ریزی شود.
این امر می تواند بر اساس مواردی از قبیل کاربرد هوای فشرده،
پیچیدگی سیستم توزیع (به عنوان مثال طول و یا انشعابات آن) یا اتصال به خطرات احتمالی آلودگی انجام شود.
در هر صورت نمونه گیری باید به گونه ای انجام شود که به خودی خود ایمن باشد و در معرض خطر آلودگی خارجی ناخواسته قرار نگیرد.
روش اندازه گیری انتخاب شده باید به گونه ای انتخاب شود که مشخصات تعریف شده مطابق با استاندارد GMP تعیین شوند.
انجام نکته آخر آسان نیست؛
زیرا برای پارامتر های جداگانه ذرات، میزان رطوبت و روغن
و همچنین گرفتن یک نمونه مطمئن برای میکروب های موجود در هوا، نیاز به تعداد زیادی فناوری اندازه گیری مختلف دارید
و باید از روش های نمونه گیری مختلف استفاده شود.
با توجه به چالش های موجود، استفاده از دستگاه اندازه گیری مناسب برای نظارت بر پارامتر های فیزیکی سیستم های هوای فشرده بسیار مهم است.
تجزیه و تحلیل کیفیت هوای فشرده
اطمینان از عملکرد سنسور ها یکی از چالش های اصلی در برخورد با فناوری اندازه گیری مربوط به بازرسی کیفیت گاز های سازگار با GMP است.
در اینجا نیز یک شرط GMP ضروری است که سنسور های اندازه گیری مورد استفاده، کالیبراسیون منظم را انجام دهند.
پس مهم است که قابلیت ردیابی بر اساس استاندارد ملی که در آن همه دستگاه های اندازه گیری باید با بالاترین دقت از یک متغیر اندازه گیری شده فیزیکی نمونه برداری کنند، تضمین شود.
کلیه کالیبراسیون های انجام شده باید با الزامات دستورالعمل های EU-GMP مطابقت داشته باشد
و باید مطابق با روش مستند سازی خوب Good Documentation Practice ثبت شود.
اطمینان از تولید ایمن
GMP در سیستم های هوای فشرده تعاملی مبتنی بر ریسک بین تعریف پارامتر های کیفیت
و اجرای آنها در یک فناوری مناسب برای تولید و توزیع است.
اما تنها صلاحیت مطابق با GMP و نیز نمونه برداری منظم می تواند از خطر آلودگی دارویی جلوگیری کند.[/vc_column_text][/vc_column][/vc_row]

